«Химия – это область чудес, в ней скрыто счастье человечества, величайшие завоевания разума будут сделаны именно в этой области».
А.М. Горький
Наиболее точную и полную модель строения атома предложил Эрнест Резерфорд, хотя понятие «атом» было известно еще в античном мире. Свою модель строения атома ученый назвал планетарной, потому что атом как крошечная Солнечная система, в центре которого ядро, а вокруг ядра вращаются электроны.
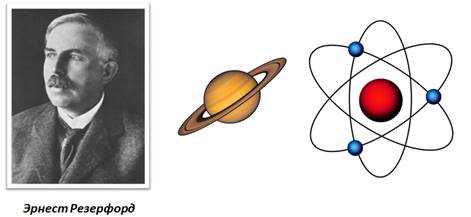
Крошечное ядро состоит из элементарных частиц – протонов и нейтронов. Рассмотрим таблицу, в которой указан символ этой частицы, её масса и заряд.
Состав ядра
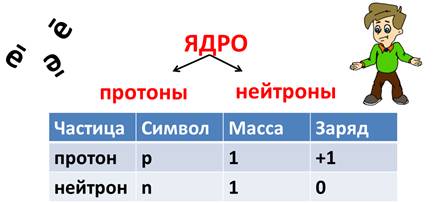
Из таблицы видно, что протон имеет заряд +1, масса протона равна 1, как и у водорода, поэтому он имеет символ р (пэ). Нейтроны тоже имеют массу равную 1, не имеют заряда, он равен 0 и обозначаются буквой n (эн). Электроны обозначаются буквой е, заряд их равен -1, т.к. масса их ничтожна мала, то ей можно пренебречь.
Сумма чисел протонов и нейтронов называется массовым числом и обозначается буквой А, которая численно равна относительной атомной массе, округленной до целого значения.
Для того чтобы определить число протонов и электронов, достаточно знать порядковый номер элемента. Например, у атома фосфора порядковый номер 15, значит у него 15 протонов в ядре, 15 электронов в атоме.

Для нахождения числа нейтронов можно использовать следующую формулу:
N = A – Z
т.к. A = Z + N, где N – число нейтронов, а Z – число протонов.
Несмотря на то, что атом очень малы, швейцарские учёные Биннинг и Рорер с помощью сканирующего микроскопа смогли увидеть реальные молекулы и атомы, в последствие им дали Нобелевскую премию за это достижение. Сканирующие микроскопы могут увеличивать объект в 100 млн. раз, т.е. позволяет увидеть частицы размером всего 10-9 м. Такие частицы называются наночастицами.

 Получите свидетельство
Получите свидетельство Вход
Вход




 0
0 25204
25204

